Diagnose og behandling av Barretts øsofagus (BØ) er basert på European Society of Gastrointestinal Endoscopy (ESGE) guidelines fra 2023 (Weusten et al., 2023).
Gastroskopi er primærundersøkelsen ved mistanke om kreft i spiserør og magesekk.
Gastroskopi
Gastroskopi med biopsi skal utføres som første prosedyre ved utredning av kreft i spiserør og magesekk. Høyoppløsningsendoskopi og visuell kromoendoskopi brukes til å oppdage små lesjoner, i øsofagus kan også bruk av fortynnet mateddik (Barretts øsofagus BØ) og Lugols oppløsning (plateepitel) være aktuelt. Ved endoskopisk mistanke om kreft, men negative biopsier, skal endoskopi og biopsier gjentas. Om vedvarende mistanke om kreft til tross for negativ re-biopsi, bør videre utredning med endoskopisk reseksjon og eventuelt EUS utføres.
Endoskopirapporten skal inneholde følgende informasjon:
- Øsofagus. Tumors eksakte beliggenhet målt i cm fra tannrekken og fra den gastroøsofageale overgangen («top of gastric fold», GØ-overgang), samt sirkulær utbredelse, må angis. Ved hernie angis diafragmakanten. Siewerts klassifisering bør her benyttes, se bilde i kirurgikapittelet. Ved Barretts øsofagus angis øvre og nedre begrensning etter Praha-klassifikasjonen (CM klassifisering). Endoskopisk overvåkning av Barret slimhinne skal fotodokumenteres
- Ventrikkel. Lokalisasjon med proksimal og distal begrensning og avstand til kardia og/eller pylorus. Ved distale svulster må bulbus duodeni beskrives. Lokaliserte forandringer i øsofagus og ventrikkel bør beskrives i samsvar med Paris klassifikasjonen. Patologiske funn skal fotodokumenteres.
FIGUR KOMMER
Det er få pasienter med kreft i tidlig stadium. Alle pasienter med kreft, sikker dysplasi, fra og med lavgradig dysplasi (LGD) og ikke-dysplastisk BØ (> 10cm) bør henvises (Weusten et al., 2023).
Endoskopisk behandling bør foregå ved samme universitetssykehus som utfører den kirurgiske behandlingen (Weusten et al., 2023). Pasienter som vurderes for endoskopisk behandling (reseksjon og/eller ablasjon) bør diskuteres på MDT møte. MDT møtet beslutter videre utredning og behandling (Weusten et al., 2023).
De europeiske retningslinjene for Barretts øsofagus (ESGE) beskriver krav til kompetanse, og at en prospektiv registrering av pasientene gjøres i en database (Weusten et al., 2023). Dette bør følges også i Norge.
Øsofagus
Barretts øsofagus (BØ) er en premalign tilstand som disponerer for høygradig dysplasi (HGD) og adenokarsinom (AK) i spiserøret.
For å stille diagnosen BØ må forandringene ved gastroskopi være av minst 1 cm lengde og inneholde den typiske intestinale metaplasien ved histopatologisk undersøkelse (Weusten et al., 2023). Som et alternativ til endoskopi kan børstebasert cytologi (Cytosponge) være et alternativ for å stille BØ diagnosen hos noen pasienter (Weusten et al., 2023).
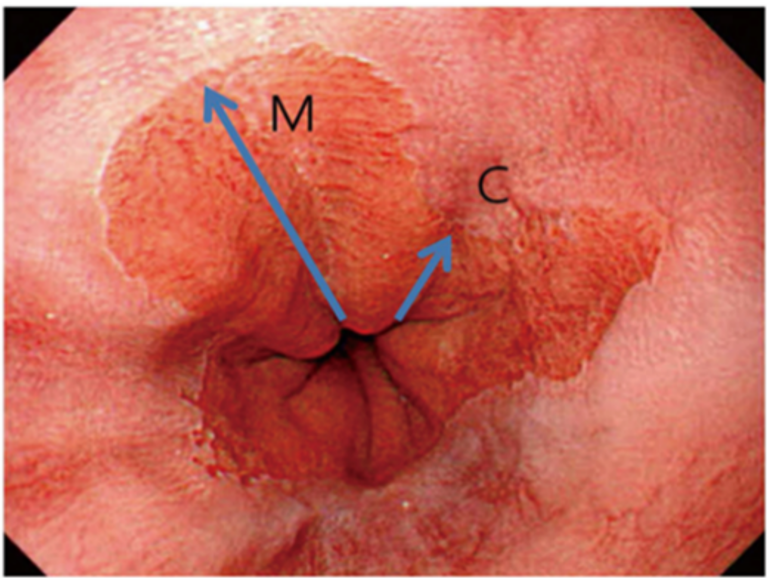
Ved gastroskopi må CM-klassifikasjonen anvendes (Praha kriteriene), der C er sirkulær og M maksimal utbredelse. Funnet må dokumenteres med et bilde der også lokaliserte forandringer innenfor BØ dokumenteres og angis etter Paris klassifikasjonen. Ved BØ skal synlige forandringer biopseres, fulgt av 4-kvadrant biopsier hver 2. cm innenfor BØ på nummererte glass.
Alle synlige forandringer innenfor BØ skal reseseres for å oppnå optimal histopatologisk diagnostikk/staging. Funn av lavgradig dysplasi (LGD) anbefales kontrollert etter seks måneder med PPI og bekreftet av en erfaren gastropatolog. Om dysplasi ikke kan bekreftes, anbefales ny kontroll etter ett år. Etter to negative kontroller, standard overvåking - dvs avhengig av BØs lengde. Om derimot LGD bekreftes, bør pasienten tilbys ablasjon; radiofrekvensablasjon (RFA) eller kryoablasjon. Om pasienten ikke allerede er i et pakkeforløp, bør dette startes ved HGD.
Ved fravær av dysplasi skal BØ med lengde 1–3 cm kontrolleres etter 5 år, 3–10 cm etter 3 år. Om BØ lengde er ≥10 cm bør pasienten henvises til et universitetssykehus som utfører spiserørskirurgi. Etter fylte 75 år og uten tidligere forekomst av dysplasi, kan det vurderes å avslutte endoskopisk overvåkning. Ved uviss (indefinite) dysplasi tas kontroll biopsier etter 6 måneder med optimalisert refluksbehandling (PPI).
Magesekk
Om biopsitaking med gastroskop ikke avklarer mistanken om kreft, kan endoskopisk ultralyd (EUS) kombinert med dypere biopsier være til hjelp, i tillegg til CT ventrikulografi.
Pasienter med adenokarsinom lokalisert til mukosa (T1a) eller submukosa (T1b) betegnes kreft i tidlig stadium uavhengig av eventuelle lymfeknutemetastaser. Ved fravær av lymfeknutemetastaser bør pasienter med T1a vurderes med tanke på endoskopisk behandling, som hos majoriteten av pasientene vil gi samme overlevelse som ved gastrektomi, men med betydelig lavere morbiditet. Ved T1b kan også endoskopisk behandling være aktuelt.
Forekomsten av kreft i tidlig stadium er i Europa rapportert til mellom 4 og 10% av alle nye tilfeller av ventrikkelcancer – omregnet 16 til 39 nye tilfeller årlig i Norge (Hauge et al., 2023). For at endoskopisk behandling skal være aktuelt må tumor være teknisk mulig å fjerne og sannsynligheten for lymfeknutemetastaser må være minimal.
Jo større tumor, jo dypere den vokser, lav differensieringsgrad og hvorvidt det foreligger innvekst i blod- eller lymfekar er alle faktorer som øker sannsynligheten for lymfeknutemetastaser.
Diagnostikk baserer seg på gastroskopi ved en erfaren endoskopør og bruk av virtuell kromoendoskopi, for eksempel Narrow Band Imaging (NBI). Bruk av endoskopisk ultralyd (EUS) for T-stadium kan være nyttig, men anbefales ikke rutinemessig (over-/underestimeres), spesielt ved lesjoner som vurderes endoskopisk resektable (Pimentel-Nunes et al., 2022). Derimot er den beste undersøkelsen for T-stadium endoskopisk reseksjon i diagnostisk øyemed, som ikke forhindrer eventuelt senere kirurgi (Hauge et al., 2023).
Endoskopisk ultralyd (EUS) kan være nyttig for T-staging ved utredning av kreft i spiserør og magesekk. Prosedyren kan være til hjelp ved endoskopisk mistanke om dyp submukosal vekst, både for T-stadium og mtp lymfeknutemetastaser (Pimentel-Nunes et al., 2022). I tillegg kan EUS-FNA/B av lokale lymfeknuter og naboorganer utføres. Ved kreft i tidlig stadium (HGD, T1a) anbefales ikke EUS rutinemessig grunnet betydelig over- og underestimering (Pimentel-Nunes et al., 2022).