Medisinsk inoperable pasienter, eller pasienter som ikke ønsker kirurgi, i stadium II uten lymfeknutemetastaser bør vurderes for stereotaktisk stråleterapi (se avsnitt «Stereotaktisk strålebehandling» i Strålebehandling). I stadium II med N1-sykdom er konkomitant kjemoterapi etterfulgt av immunterapi (som stadium III) et alternativ til kirurgi (se avsnitt «Konkomitant kjemoradioterapi etterfulgt av immunterapi»).
Ubehandlet er prognosen i stadium III dårlig med 2 års overlevelse på 0-4 %, mens en metaanalyse viste ca 15 % 5-års overlevelse etter kombinert kjemoradioterapi (Aupérin et al., 2010). Konsoliderende immunterapi med preparatet durvalumab øker overlevelsen betydelig (se under).
Utfyllende informasjon om strålebehandling finnes i Faglige anbefalinger for strålebehandling ved ikke-småcellet lungekreft.
Konkomitant (samtidig) kjemoradioterapi er funnet mer effektiv enn sekvensiell behandling (Bi & Wang, 2015). Bivirkningene ved slik behandling kan være betydelige, og pasientene må derfor selekteres nøye. MR caput og PET/CT inngår i utredningen (se Oversikt utredning av lungekreft i spesialisthelsetjenesten). Ved tvil om pasienten er i stand til å gjennomføre konkomitant behandling, bør heller sekvensiell behandling velges, alternativt stråleterapi alene (D. De Ruysscher et al., 2009).
Konkomitant kjemoradioterapi etterfulgt av immunterapi
Ved konkomitant behandling gis kjemoterapi samtidig med strålebehandling, 2 Gy x 30-33. Ved store svulster som ikke ligger i nærheten av kritiske strukturer (hjerte, øsofagus, plexus) kan man overveie å eskalere dosen til 70 Gy. Pasienter som ikke er kandidat for kjemoradioterapi tilbys strålebehandling alene med 2 Gy x 33 – 35, totalt 66 – 70 Gy. Det er ikke konsensus hvilket kjemoterapiregime som er best (Bi & Wang, 2015). Vanligst brukt er 2 kurer platinumbasert kjemoterapi gitt med 3 ukers intervall. I Norge anbefales PV-regimet (se avsnitt «PV-regime» i Behandling av ikke-operabel begrenset sykdom, LS-SCLC), eventuelt cisplatin/vinorelbin. Første kur gis fra første eller andre strålebehandlingsdag. Det er svært begrenset med data på bruk av G-CSF ved konkomitant kjemotradioterapi ved ikke-småcellet lungekreft, og med moderne små strålefelt er trolig risikoen liten. Noen argumenterer for bruk av G-CSF ved neutropeni etter første kur, og dette er nå også implementert i enkelte internasjonale retningslinjer (Arrieta et al., 2020; Benna et al., 2020).
I en stor fase III-studie, «PACIFIC» ble opp til 12 måneders konsoliderende behandling med immunterapi med PD-L1-hemmeren durvalumab gitt til pasienter med lokalavansert ikke-resektabel sykdom etter konkomitant kjemoradiasjon (Antonia et al., 2017). Median progresjonsfri overlevelse var signifikant bedre med durvalumab versus placebo, med henholdsvis 16,8 måneder versus 5,6 måneder, p< 0.0001. Overlevelsesdata etter 34 mndr oppfølgningstid viste estimert 5-års overlevelse på 42,9 % i gruppen som fikk durvalumab mot 33,4 % i gruppen som fikk placebo (HR 0,72) (D. R. Spigel et al., 2022). Antall og alvorlighetsgrad av bivirkninger var sammenlignbare i de to armene. Pneumonitt eller strålepneumonitt hos pasienter som mottok durvalumab var for det meste lavgradig med få og et sammenlignbart antall grad 3- eller 4-tilfeller i de to gruppene.
Studien inkluderte også pasienter med EGFR- og ALK-positiv sykdom, men det er nå data som viser at immunterapi ikke er av nytte for disse pasientene (Arter & Nagasaka, 2024). EGFR-positive pasienter har nytte av EGFR-rettet behandling som beskrevet under i «Konkomitant kjemoradioterapi etterfulgt av EGFR-TKI hos EGFR-mutert NSCLC stadium III».
Durvalumab har markedsføringstillatelse til behandling av lokalavansert, inoperabel, ikke-småcellet lungekreft med PD‑L1-uttrykk ≥1 %, og med sykdom som ikke har progrediert etter platinabasert kjemoradiasjon. Denne behandlingen ble vurdert i Beslutningsforum 21.10.19 med følgende vedtak:
«Durvalumab (Imfinzi) kan innføres til behandling av lokalavansert, inoperabel ikke-småcellet lungekreft (NSCLC) hos voksne hvor tumor uttrykker PD-L1 ≥ 1 % av tumorcellene og med sykdom som ikke har progrediert etter platinabasert kjemoradiasjon.»
Durvalumab gis som intravenøs infusjon, 10 mg/kg hver 2. uke eller 1500 mg hver 4. uke, og bør startes innen 42 dager etter siste strålefraksjon. Det ble vist at tidlig oppstart korrelerer med bedre overlevelse ved at pasienter som ble randomisert innen 14 dager etter siste strålefraksjon hadde en HR=0,42, mot HR=0,81 ved randomisering senere enn 14 dager (Antonia et al., 2018). CT toraks og øvre abdomen som baseline 2-3 uker etter gjennomført kjemoradiasjon bør derfor tilstrebes. Behandlingen gis i inntil 1 år, eller til uakseptabel toksisitet (se Immunterapi: bivirkninger, behandlingsvarighet og annet) eller tilbakefall.
Skjematisk kan behandlingsopplegget framstilles som i Figur 17.
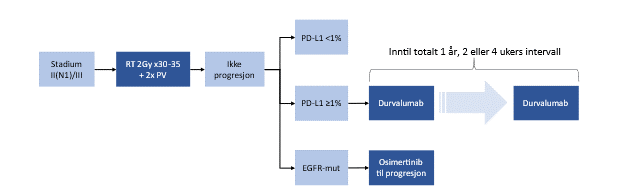
Konkomitant kjemoradioterapi etterfulgt av EGFR-TKI hos EGFR-mutert NSCLC stadium III
Pasienter med inoperabel NSCLC stadium III med påvist EGFR-mutasjon har ikke nytte av konsoliderende immunterapi som beskrevet over (Nassar et al., 2024).
I en stor fase III-studie, «LAURA» ble konsoliderende behandling med EGFR-hemmeren osimertinib gitt til pasienter med lokalavansert ikke-resektabel sykdom etter konkomitant kjemoradiasjon (Lu, Kato, et al., 2024). Median progresjonsfri overlevelse var signifikant bedre med osimertinib versus placebo, med henholdsvis 39,1 måneder versus 5,6 måneder (HR 0,16, p < 0,001). Overlevelsesdata med foreløpig umodne data viste estimert 3-års overlevelse på 84 % i gruppen som fikk osimertinib mot 74 % i gruppen som fikk placebo (HR 0,81, p = 0,53). Kumulativ insidens av CNS-metastaser etter 12 mndr var 9 % i osimertinib-gruppen, mot 36 % med placebo (Lu, Ahn, et al., 2024). Bivirkninger av grad 3 og 4 forekom hos 35 % av osimertinib-behandlede pasienter, mot 12 % i placebogruppen. Pneumonitt eller strålepneumonitt var for det meste lavgradig i begge grupper, og forekom hos 48 % i osimertinib-gruppen og 38 % i placebogruppen.
I studien ble det ikke satt noen begrensning på hvor lenge pasientene skulle stå på osimertinib, men det er rimelig at man etter en tid vurderer nytten. Eksempelvis anbefales tre års adjuvant osimertinib etter operasjon.
Osimertinib som monoterapi til behandling av voksne pasienter med lokalavansert, ikke-resekterbar NSCLC der tumor har EGFR ekson 19-delesjoner eller ekson 21 (L858R) substitusjonsmutasjoner, og der sykdommen ikke har progrediert under eller etter platinabasert kjemoradioterapi er vurdert i Beslutningsforum 16.06.25 med følgende vedtak:
- «Osimertinib (Tagrisso) innføres som monoterapi til behandling av voksne pasienter med lokalavansert, ikke-resekterbar ikke-småcellet lungekreft (NSCLC) der tumor har EGFR ekson 19-delesjoner eller ekson 21 (L858R) substitusjonsmutasjoner, og der sykdommen ikke har progrediert under eller etter platinabasert kjemoradioterapi.»
- «Det forutsetter at prisen er lik eller lavere enn den prisen som er grunnlaget for denne beslutningen.»
- «Behandlingen kan tas i bruk fra beslutningstidspunktet.»
Også pasienter som av ulike grunner ikke har fått kjemoterapi bør få tilbud om osimertinib, og ved progresjon er også osimertinib aktuell som førstelinje systemisk behandling. Se Figur 17.
Sekvensiell kjemoradioterapi stadium III
Ved tvil om toleransen for konkomitant kjemoradioterapi kan sekvensiell behandling gis med kjemoterapi før strålebehandling. Et platinumbasert kjemoterapi regime er anbefalt, 2 kurer før start av stråling. Immunterapi med durvalumab i inntil 1 år som beskrevet over kan vurderes også i disse situasjonene (sekvensiell kjemoterapi og radioterapi) utfra publiserte data (Garassino et al., 2022). Pasienter som ikke er kandidat for tillegg med kjemoterapi tilbys strålebehandling alene med 2 Gy x 33 – 35.
Anbefaling - kjemoradioimmunoterapi ved stadium III
- Konkomitant kjemoradioterapi anbefales: 2 Gy x 30-33 med to platinumbaserte cellegiftkurer med tre ukers intervall under strålebehandling.
- Durvalumab gis ved EGFR-/ALK-negativ sykdom som ikke har progrediert etter kjemoradioterapi, og med PD-L1-uttrykk i ≥ 1 % av tumorcellene: 10 mg/kg hver 2. uke eller 1500 mg hver 4. uke i inntil 12 måneder.
- Osimertinib kan gis inntil progresjon hos pasienter med EGFR-positiv sykdom som ikke har progrediert etter kjemoradioterapi, eller der det er behov for systemisk behandling pga progresjon.